Monosaccharide – Eigenschaften und Reaktionen

in nur 12 Minuten? Du willst ganz einfach ein neues
Thema lernen in nur 12 Minuten?
-
 5 Minuten verstehen
5 Minuten verstehen
Unsere Videos erklären Ihrem Kind Themen anschaulich und verständlich.
92%der Schüler*innen hilft sofatutor beim selbstständigen Lernen. -
 5 Minuten üben
5 Minuten üben
Mit Übungen und Lernspielen festigt Ihr Kind das neue Wissen spielerisch.
93%der Schüler*innen haben ihre Noten in mindestens einem Fach verbessert. -
 2 Minuten Fragen stellen
2 Minuten Fragen stellen
Hat Ihr Kind Fragen, kann es diese im Chat oder in der Fragenbox stellen.
94%der Schüler*innen hilft sofatutor beim Verstehen von Unterrichtsinhalten.
Grundlagen zum Thema Monosaccharide – Eigenschaften und Reaktionen
Monosaccharide sind löslich in Wasser und nicht löslich in unpolaren Lösungsmitteln. Sie schmecken süß und karamellisieren beim Erwärmen. D-Glucose gehört zu den reduzierenden Zuckern. Sie reagiert mit Tollens Reagenz oder Fehling-Lösung. Dabei wird sie zu D-Gluconsäure oxidiert. Es gibt eine Variante im Zellstoffwechsel, bei der D-Glucoronsäure entsteht. Reduktion von D-Glucose gibt D-Sorbit (Süßstoff), D-Mannose liefert das optisch nicht aktive Mannitol (Mannit). Letzteres ist eine meso-Form.
Transkript Monosaccharide – Eigenschaften und Reaktionen
Guten Tag und herzlich willkommen. Dieses Video heißt Monosaccharide - Eigenschaften und Reaktionen. Es wäre schön, wenn Du bereits folgende Vorkenntnisse besitzt: Du solltest schon umfangreichere Vorstellungen über Kohlenhydrate und Monosaccharide besitzen. Du solltest mit den wichtigsten organischen Verbindungsklassen, wie Aldehyden und Ketonen vertraut sein. Außerdem hast Du klare Vorstellungen über die chemischen Begriffe Oxidation und Reduktion. Mein Ziel ist es, Euch in diesem Video die wesentlichen Eigenschaften und Reaktionen der Monosaccharide vorzustellen. Das Video ist in 4 Abschnitte eingeteilt: 1. Eigenschaften 2. Oxidation zu Zuckersäuren 3. Reduktion zu Zuckeralkoholen und 4. Zusammenfassung.
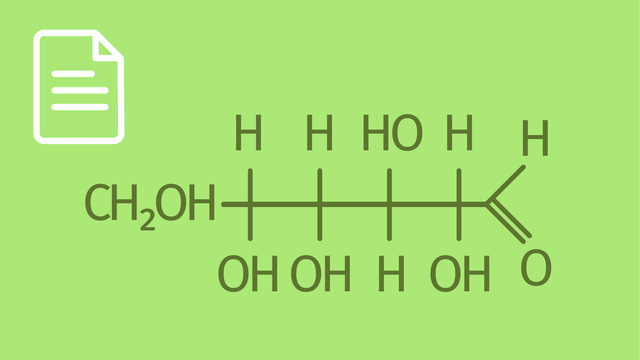
Eigenschaften ich möchte die Eigenschaften der Monosaccharide exemplarisch an dieser Hexose demonstrieren. Die Aufmerksamen von Euch werden jetzt schon wissen, dass es sich hierbei um D-Glucose handelt. Das Molekül hab ich in der Fischerprojektion dargestellt. Wir haben bereits gelernt, dass es sich bei den Monosacchariden um Polyalkohole handelt. Die Hydroxygruppen sind hydrophil. Daraus resultiert die gute Löslichkeit von Monosacchariden in Wasser. Im Gegensatz dazu sind Monosaccharide in typischen organischen Lösungsmitteln, die hydrophob sind, nur schwer oder gar nicht löslich. Monosaccharide sind in der Regel süß und werden partiell für die Zubereitung von Süßspeisen verwendet. Beim moderaten Erhitzen von Monosacchariden kommt es zur Karamellisierung.
Oxidation zu Zuckersäuren Monosaccharide können durch entsprechende Reagenzien oxidiert werden. Eine Möglichkeit ist die Oxidation mit Tollens-Reagenz. Das ist ammoniakalische Silbernitratlösung. Die Aldehydgruppe des Monosaccharids wird zur Carboxylgruppe oxidiert, aus den Silberionen entsteht elementares Silber. Aus D-Glucose entsteht D-Gluconsäure. D-Gluconsäure entsteht auch, wenn man anstelle von Tollens-Reagenz Fehling'sche Lösung verwendet. Die erfolgreiche Reaktion durch Tollens-Reagenz wird durch den bekannten Silberspiegel angezeigt. Man sagt, D-Glucose ist ein reduzierender Zucker. Neben D-Glucose ist auch D-Fructose ein reduzierender Zucker. Unter den basischen Bedingungen der Reaktion wird aus der Ketose eine Aldose, die selber reduzierende Eigenschaften aufweist. Saccharose hingegen ist kein reduzierender Zucker. Alternativ zur Oxidation der D-Glucose zur D-Gluconsäure findet eine andere Reaktion statt. Diese trifft man beim Zellstoffwechsel an. Interessanterweise wird dabei die Aldehydgruppe oben im Molekül von der Oxidation nicht berührt. Anstelle dessen wird die Hydroxmethylgruppe ganz unten im Molekül zur Carboxylgruppe oxidiert. Das Reaktionsprodukt ist Glucoronsäure, genauer D-Glucoronsäure. Obwohl das Kohlenstoffatom unten im Molekül die höchste Oxidationsstufe besitzt wird die Fischerprojektion aus Übersichtsgründen beibehalten.
Reduktion zu Zuckeralkoholen Bei der Reduktion von D-Glucose findet eine Umwandlung der Aldehydgruppe, oben im Molekül zu einer Hydroxymethylgruppe statt. Aus einem Aldehyd entsteht ein Alkohol. Das Reaktionsprodukt nennt man D-Glucitol. Es ist besser unter dem Namen D-Sorbit bekannt. Das ist ein Zuckerersatzstoff. D-Mannose kann ebenfalls reduziert werden. Es bildet sich Mannitol. Besser unter dem Namen Mannit bekannt. Das Molekül des Mannits hat eine interessante Eigenschaft. Es verfügt genau wie das Molekül der D-Mannose über vier chirale Zentren. Wenn ich die funktionelle Gruppe jetzt oben umfärbe, so seht Ihr vielleicht, dass es hier eine Symmetrie-Eigenschaft gibt. Das Molekül ist antisymmetrisch bezüglich der eingezeichneten Spiegelebene S. Das hat zur Folge, dass der obere Teil des Moleküls polarisiertes Licht in die eine Richtung (ich hab hier bedingt entgegen den Uhrzeigersinn aufgeschrieben) dreht, während der untere Teil des Moleküls das Licht genau um den gleichen Betrag in die andere Richtung dreht. Also einmal nach links und einmal nach rechts, jeweils um dem gleichen Betrag. Im Ergebnis ist die Gesamtdrehung null. Das bedeutet, dass das Molekül optisch nicht aktiv ist. Wir haben es hier genauso (erinnert Euch an das Video mit Weinsäure) mit einer meso-Form zu tun.
Zusammenfassung Glucose und andere Monosaccharide sind hydrophile chemische Verbindungen und daher gut wasserlöslich, schwer jedoch in organischen Lösungsmitteln. Sie sind süß und karamellisieren. Oxidationen von Monosacchariden mit geeigneten Oxidationsmitteln, wie Tollens-Reagenz oder Fehlingscher-Lösung liefern entsprechende Zuckersäuren. Eine Möglichkeit ist die Entstehung von D-Gluconsäure. Beim Zellstoffwechsel ist alternativ eine andere interessante Reaktion möglich. Hierbei wird die Aldehydgruppe der D-Glucose nicht angegriffen. Im Gegensatz dazu wird die Hydroxymethylgruppe am unteren Teil des Moleküls zur Carboxylgruppe oxidiert. Die gebildete Zuckersäure heißt D-Glucoronsäure. Reduktion der Monosaccharide liefert Zuckeralkohole. Aus D-Glucose entsteht D-Glucitol, besser unter dem Namen D-Sorbit bekannt. Auch Mannose ist reduzierbar, bildet Mannit, das eine meso-Form darstellt, die optisch nicht aktiv ist.
Ich danke für die Aufmerksamkeit. Alles Gute. Auf Wiedersehen.
Monosaccharide – Eigenschaften und Reaktionen Übung
-
Bestimme, in welchen Lösungsmitteln Monosaccharide löslich sind.
TippsPolares löst sich in polaren Lösungsmitteln und Unpolares in unpolaren Lösungsmitteln.
LösungIn welchem Lösungsmittel ein Stoff löslich ist, hängt generell mit den Stoffeigenschaften zusammen. Man kann Stoffe allgemein in zwei Klassen unterteilen: polare und unpolare Stoffe. Hier gilt die Regel, dass Gleiches sich in Gleichem löst. Wie kann man nun überprüfen, ob ein Stoff polar oder unpolar ist? Ein polarer Stoff verfügt häufig über ein Dipolmoment oder ist eine ionische Verbindung (Beispiele wären hier Wasser und Salzverbindungen). Hier findet eine Wechselwirkung der Polaritäten statt, sodass sich die Stoffe lösen. Bei unpolaren Stoffen gilt genau das Gegenteil. In unserem Beispiel lässt sich also erkennnen, dass die Carbonyl- und Hydroxygruppen in jedem Monosaccharid polar sind, sodass sich einfache Zucker stets in polaren Lösungsmitteln, wie Wasser oder Cola, gut lösen.
-
Erkenne die funktionellen Gruppen der Monosaccharide.
TippsEin Zucker ist formal auch ein Mehrfachalkohol.
LösungMonosaccharide sind lange Kohlenstoffketten, welche verschiedene funktionelle Gruppen besitzen, die ihre chemischen Eigenschaften bestimmen. Zucker sind sehr gut wasserlöslich. Das ist bedingt durch die vielen, polaren, funktionellen Gruppen. Zum einen befinden sich eine Reihe von Hydroxygruppen (-OH) am Molekül. Diese sind die charakteristische funktionelle Gruppe der Alkohole, weshalb Zucker auch als Mehrfachalkohole betrachtet werden können.
In der Kettenform besitzen einige Zuckermoleküle (Aldosen) auch eine Aldehydgruppe (-CHO). Aus diesem Grund können mit den Aldehydnachweisen, die auf der reduzierenden Wirkung der Aldehydgruppe beruhen, auch Zucker nachgewiesen werden.
-
Bestimme Oxidationsmittel und Reduktionsmittel für Monosaccharide.
TippsMetallhydride (${ Me }_{ x }{ H }_{ x }$) sind oftmals gute Reduktionsmittel.
Verbindungen mit Sauerstoff sind meist gute Oxidationsmittel.
LösungMonosaccharide haben die Eigenschaft sich sowohl oxidieren als auch reduzieren zu lassen. Hierbei bildet sich bei einer Oxidation die entsprechende Carbonsäure. Ebenso wird bei einer Reduktion der entsprechende Alkohol gebildet.
$\mathrm{Alkohol \ \xrightarrow{Ox.} \ Aldehyd \ \xrightarrow{Ox.} \ Carbonsäure}$
Nun muss man jedoch wissen, was als Oxidationsmittel und was als Reduktionsmittel genutzt werden kann, wenn man diese Reaktionen herbeiführen möchte. Oxidationsmittel sind Stoffe mit einer sehr hohen Oxidationszahl durch den Sauerstoff. Dazu zählen in unserem Beispiel die Salpetersäure sowie das Kaliumpermanganat. Wasserstoffperoxid ist ebenfalls ein häufig genutztes und starkes Oxidationsmittel. Dagegen sind Reduktionsmittel oftmals Metallhydride. Dazu zählt im Beispiel das Natriumborhydrid. Hydrazin ($N_2H_4$) und Natriumamalgam ($Na _xHg_x$) sind sehr starke Reduktionsmittel, die oftmals auch in der organischen Chemie genutzt werden.
-
Erkläre, warum die Fehling-Probe für Zuckernachweise verwendet werden kann.
TippsMonosaccharide können den Reaktionspartner reduzieren.
Was entsteht durch Oxidation der Aldehydgruppe?
Bei der Oxidation werden Elektronen frei und die Oxidationszahl steigt.
LösungDie Fehling-Probe ist ein wichtiger Nachweis von Reduktionsmitteln und kann besonders Monosaccharide nachweisen. Hierbei bilden Kupfersulfat und Kaliumnatriumtartrat einen Komplex, in dem das Kupfer in der Oxidationsstufe II vorliegt. Dieses wird dann mit der zu untersuchenden Substanz vermischt und erwärmt, sodass das Kupfer schließlich im Fall der Monosaccharide von der Aldehygruppe zu Kupfer(I) reduziert wird. Gleichzeitig wird die Aldehydgruppe zu einer Carbonsäure oxidiert. Die gesamte pH-Umgebung muss dabei basisch sein, damit die Oxidation zur Carbonsäure stattfinden kann. Die gesamte Redoxreaktion lautet:
$R-CHO + 2~Cu^{2+} + 5~OH^- \rightarrow R-COO^- + Cu_2O + 3~H_2O$.
-
Nenne Eigenschaften der Monosaccharide.
TippsSaccharide, welche oxidiert werden, bekommen eine Carbonsäuregruppe.
Die Reduktion einer Aldehydgruppe bedeutet, dass sie zum Alkohol reduziert wird.
LösungMonosaccharide haben auf Grund ihrer Struktur viele charakteristische Eigenschaften. Zum einen sind sie durch die hydrophilen Hydroxygruppen sehr gut in Wasser und ähnlichen polaren Lösungsmitteln löslich und unlöslich in unpolaren, organischen Lösungsmitteln. Wenn man Monosaccharide erwärmt, dann karamellisieren sie, was sich auch Bäcker und Köche zunutze machen.
Durch die Aldehydgruppe lassen sich Zucker, wie andere Aldehyde, oxidieren und reduzieren. Werden sie oxidiert, reagiert die Aldehydgruppe zu einer Carbonsäure. So wird beispielsweise aus D-Glucose D-Gluconsäure. Auch eine Reduktion der Aldehydgruppe ist möglich. Diese reagiert nun jedoch zu einer Alkoholgruppe. Aus D-Glucose wird nun D-Glucitol oder auch D-Sorbit, welches ein beliebter Zuckerersatzstoff ist.
-
Bestimme die Stoffklasse folgender Verbindungen.
TippsWenn eine Carbonylgruppe reduziert wird, entsteht ein Alkohol.
LösungZucker, also Monosaccharide, können sowohl oxidiert als auch reduziert werden. Bei der Oxidation entsteht eine sogenannte Zuckersäure. Merkmal der Zuckersäuren ist, dass die Aldehyd-Gruppe oder eine endständige Alkohol-Gruppe zur Carboxygruppe oxidiert wird.
$\mathrm{R-CHO \ \xrightarrow{Ox.} \ R-COOH}$
Das gewählte Beispiel ist die Gluconsäure, die bei der Oxidation von Glucose entsteht. Bei der Reduktion von einfachen Zuckern entsteht ein sogenannter Zuckeralkohol oder auch Alditol. Hier wird die Carbonylgruppe zu einem Alkohol reduziert.
$\mathrm{R-CHO \ \xrightarrow{Red.} \ R-{CH}_{2}OH}$

Grundbaustoffe der Nahrung – Kohlenhydrate, Eiweiße und Fette

Monosaccharide

Glucose und Fructose

Glucose – Kette oder Ring?

Monosaccharide mit 3 bis 6 C-Atomen

Monosaccharide – Nomenklatur und Stereochemie

Monosaccharide – Eigenschaften und Reaktionen

Pyranosen und Furanosen

D-Ribopyranose und D-Ribofuranose

Sesselform-Schreibweise der Pyranosen

Halbacetal- und Acetalbildung

Disaccharide

Disaccharide – Besondere Glykoside

Reduzierende und nichtreduzierende Disaccharide

Saccharose und Maltose

Polysaccharide

Polysaccharide – Cellulose, Stärke, Glykogen

Stärke und Cellulose

Nachweis von Kohlenhydraten

Moleküldarstellungen von Kohlenhydraten

Zuckerderivate
Glykoside und glykosidische Bindung

Glykolipide und Glykoproteine

Hyaluronsäure, Heparin, Chitin
9'178
sofaheld-Level
6'600
vorgefertigte
Vokabeln
7'642
Lernvideos
35'607
Übungen
32'354
Arbeitsblätter
24h
Hilfe von Lehrkräften

Inhalte für alle Fächer und Schulstufen.
Von Expert*innen erstellt und angepasst an die Lehrpläne der Bundesländer.
Testphase jederzeit online beenden
Beliebteste Themen in Chemie
- Periodensystem
- Ammoniak Verwendung
- Entropie
- Salzsäure Steckbrief
- Kupfer
- Stickstoff
- Glucose Und Fructose
- Salpetersäure
- Redoxreaktion
- Schwefelsäure
- Natronlauge
- Graphit
- Legierungen
- Dipol
- Molare Masse, Stoffmenge
- Sauerstoff
- Elektrolyse
- Bor
- Alkane
- Verbrennung Alkane
- Chlor
- Elektronegativität
- Tenside
- Toluol, Toluol Herstellung
- Wasserstoffbrückenbindung
- Fraktionierte Destillation Von Erdöl
- Carbonsäure
- Ester
- Harnstoff, Kohlensäure
- Reaktionsgleichung Aufstellen
- Redoxreaktion Übungen
- Stärke und Cellulose Chemie
- Süßwasser und Salzwasser
- Katalysator
- Ether
- Primärer Alkohol, Sekundärer Alkohol, Tertiärer Alkohol
- Van-der-Waals-Kräfte
- Oktettregel
- Kohlenstoffdioxid, Kohlenstoffmonoxid, Oxide
- Alfred Nobel
- Wassermolekül
- Ionenbindung
- Phosphor
- Saccharose Und Maltose
- Aldehyde
- Kohlenwasserstoff
- Kovalente Bindung
- Wasserhärte
- Peptidbindung
- Fermentation




 5 Minuten verstehen
5 Minuten verstehen
 5 Minuten üben
5 Minuten üben
 2 Minuten Fragen stellen
2 Minuten Fragen stellen

 Bereit für eine echte Prüfung?
Bereit für eine echte Prüfung?












Eine sehr gute und prinzipielle Frage.
L-Glucose gibt es in der Natur nicht. Sie kann synthetisiert werden, ist aber für die Energiegewinnung unbrauchbar.
Energetisch dürfte es zwischen den beiden Isomeren der Glucose, D und L, keinen Unterschied geben. Vor einigen Jahren gab es eine quantenchemische Untersuchung an der Technischen Universität Berlin. Sie konnte zeigen, dass es minimale energetische Unterschiede zwischen bestimmten Isomeren D und L gibt. Vielleicht ist das der Grund für die ausschließliche Bildung von D.
Man vermutet aber auch, dass die natürliche Bildung von D zufällig geschehen ist. Die Organismen haben sich dann entsprechend dieser Struktur entwickelt, weil nur so der Stoffwechsel möglich ist.
Ich hoffe, dass dich die Antwort so einigermaßen zufrieden stellen konnte.
Alles Gute
Hallo! Was ist denn eigentlich das Grund dafür, dass die meisten Zucker D-konfiguriert sind? lg