Fette
Fette bringen dem Körper viel Energie, sie sind natürliche Ester aus gesättigten oder ungesättigten Fettsäuren und dem Alkohol Glycerin.
Beliebteste Videos und Lerntexte
Jetzt mit Spass die Noten verbessern
und sofort Zugriff auf alle Inhalte erhalten!
30 Tage kostenlos testenInhaltsverzeichnis zum Thema
Vorkommen und Aufbau
Fette sind ein Grundbestandteil unserer Nahrung. Fette sind organische Ester. Diese Ester entstehen durch eine Reaktion von einem Alkohol mit einer Carbonsäure. Den Alkohol eines Fettes stellt immer Glycerin dar. Glycerin ist ein dreifacher Alkohol. Hier siehst du ihn in einer Strukturformel dargestellt auf der linken Seite des Bildes.
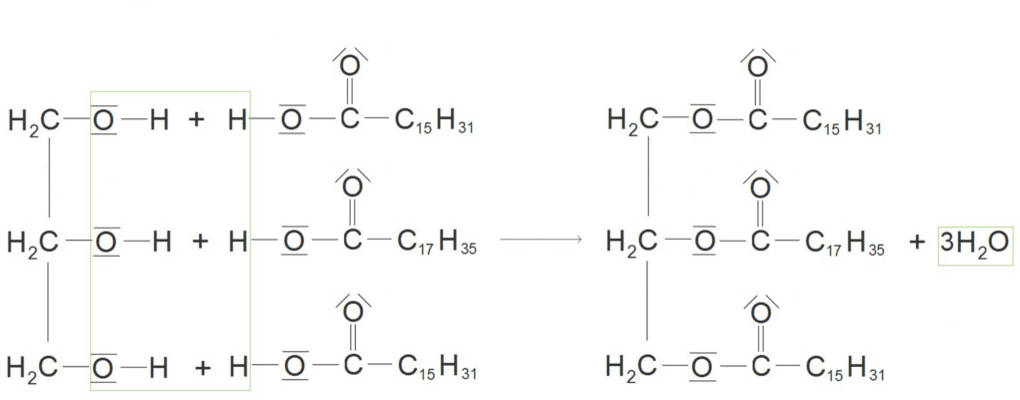
Es handelt um ein Propanol. Nach IUPAC lautet der systematische Name Propan-1,2,3-ol. Mit jeder Hydroxyl-Gruppe hat eine Carbonsäure unter Wasserabspaltung reagiert. Bei Fetten sitzen an jeder der Alkohol-Gruppen eine Fettsäure. Diese Fettsäuren sind langkettig und aliphatisch. Die Moleküle sind unverzweigt. Es gibt gesättigte und ungesättigte Fettsäuren. Gesättigte Fettsäuren kommen häufig bei tierischen Fetten vor. Diese Fette sind fest. Pflanzliche Fette und die von Fischen enthalten viele ungesättigte Fettsäuren. Die enthaltenen Doppelbindungen sind nicht frei drehbar. Daher nehmen ungesättigte Fettsäuren (FS) mehr Raum ein. Ungesättigte Fette sind aus diesem Grund flüssig und werden Öle genannt.

Einige wichtige Fettsäuren solltest du dir einprägen.
Die Stearinsäure $(C_{17}H_{35}COOH)$ ist eine oft vorkommende gesättigte Fettsäure.
Die Ölsäure $(C_{17}H_{33}COOH)$ ist eine einfach ungesättigte Fettsäure und
die Linolsäure $(C_{17}H_{31}COOH)$ ist eine zweifach ungesättigte Fettsäure.
Fette und Öle kommen in allen Tieren und in Pflanzen vor. Besonders ölreiche Pflanzen sind Raps und Oliven. Auch alle Samen und Nüsse enthalten Öl.
Härtung von Fetten
Bei der Herstellung von Margarine werden ungesättigte Fette katalytisch z.B. über Nickel in gesättigte Fette umgewandelt. Dies nennt man in der Lebensmittelchemie Härtung von Fetten. Hierbei werden die Doppelbindungen der ungesättigten Fette mit Wasserstoff gesättigt. Durch diesen Prozess entsteht z.B. aus einem flüssigen Fettsäureester mit drei Ölsäuren ein fester Fettsäureester mit drei Stearinsäuren. Bei diesem Prozess können aber auch trans-Fettsäuren entstehen die das Herz-Kreislaufsystem schädigen können.
Eigenschaften und Verwendung von Fetten
Die Eigenschaften von Fetten kann man aus ihrer Struktur ableiten. Je nach Struktur und Eigenschaft, können finden Fette ganz unterschiedliche Verwendung finden. Fette sind flüssig bis fest. Flüssige Fette enthalten Doppelbindungen und werden Öle genannt. Fette sind weiß oder besitzen eine gelbe Farbe. Dabei können sie trüb oder auch klar sein. Fette sind aufgrund ihrer Struktur, die viel Platz benötigt, recht weich. Sie besitzen eine Dichte kleiner als 1 $\frac {g}{cm3}$. Damit ist ihre Dichte geringer als die von Wasser. Aus diesem Grund schwimmt Fett immer an der Wasseroberfläche.
Bild: wasser und öl.jpg, Fette: Wasser und Öl im Glas
Fette sind immer Stoffgemische. Es sind viele verschiedene Fettsäuren in einem Fett enthalten. Aufgrund dieser Vielzahl an FS variieren die Eigenschaften der Fette. Fette sind sehr unpolare Verbindungen, da sie größtenteils aus Kohlenstoff und Wasserstoff aufgebaut sind. Für die Löslichkeit von Stoffen gilt der Merksatz: „Gleiches löst sich in Gleichem“.
Daher sind Fette gut löslich in unpolaren Lösemitteln wie Benzin und Diesel. In Wasser und kurzkettigen Alkoholen dagegen sind Fette nicht löslich. Fetten kommt in der Nahrung eine große Bedeutung zu. Sie liefern uns große Mengen Energie. Diese wird durch eine kontrollierte Oxidation in den Zellen gewonnen. In unserem Körper hat das Fett vielfältige Aufgaben. Am offensichtlichsten ist die Speicherung von Energie in Fettreserven. Es dient aber auch der Isolation gegen Kälte und der Dämpfung von Stößen z.B. in unseren Fußsohlen. Fette dienen als Schmiermittel. Wenn in Maschinen Metallteile aufeinander reiben, ist ein Schutzfilm von Nöten. Für diese Aufgabe gibt es spezielle Öle, die z.B. in Autos eingesetzt werden.
Hydrolyse von Fetten
Fette können auch wieder in ihre Bestandteile zerlegt werden. Dies kann beispielsweise durch eine Hydrolyse geschehen. Dabei wird das Fett durch Wasser gespalten. Die Reaktion kann katalysiert mit einer Säure oder als irreversible Reaktion einer Base ablaufen. Dabei entstehen wieder Glycerin und die Fettsäuren. Diese Reaktion wird z.B. bei der Seifenherstellung genutzt. Dafür wird dem Fett z.B. Natriumhydroxid zugegeben.

Alle Videos und Lerntexte zum Thema
Videos und Lerntexte zum Thema
Fette (11 Videos, 1 Lerntext)
Alle Arbeitsblätter zum Thema
Arbeitsblätter zum Thema
Fette (12 Arbeitsblätter)
-
 Fettsäuren
PDF anzeigen
Fettsäuren
PDF anzeigen -
 Fette und Öle
PDF anzeigen
Fette und Öle
PDF anzeigen -
 Ungesättigte Fettsäuren
PDF anzeigen
Ungesättigte Fettsäuren
PDF anzeigen -
 Fette und Öle (Basiswissen)
PDF anzeigen
Fette und Öle (Basiswissen)
PDF anzeigen -
 Fette und Öle (Vertiefungswissen)
PDF anzeigen
Fette und Öle (Vertiefungswissen)
PDF anzeigen -
 Vorkommen und Zusammensetzung natürlicher Fette
PDF anzeigen
Vorkommen und Zusammensetzung natürlicher Fette
PDF anzeigen -
 Fette – Eigenschaften (Basiswissen)
PDF anzeigen
Fette – Eigenschaften (Basiswissen)
PDF anzeigen -
 Fette – Eigenschaften (Vertiefungswissen)
PDF anzeigen
Fette – Eigenschaften (Vertiefungswissen)
PDF anzeigen -
 Analytik von Fetten (Vertiefungswissen)
PDF anzeigen
Analytik von Fetten (Vertiefungswissen)
PDF anzeigen -
 Analytik von Fetten (Expertenwissen)
PDF anzeigen
Analytik von Fetten (Expertenwissen)
PDF anzeigen -
 Hydrolyse von Fetten (Vertiefungswissen)
PDF anzeigen
Hydrolyse von Fetten (Vertiefungswissen)
PDF anzeigen -
 Hydrolyse von Fetten (Expertenwissen)
PDF anzeigen
Hydrolyse von Fetten (Expertenwissen)
PDF anzeigen
Beliebteste Themen in Chemie
- Periodensystem
- Ammoniak Verwendung
- Entropie
- Salzsäure Steckbrief
- Kupfer
- Stickstoff
- Glucose Und Fructose
- Salpetersäure
- Redoxreaktion
- Schwefelsäure
- Natronlauge
- Graphit
- Legierungen
- Dipol
- Molare Masse, Stoffmenge
- Sauerstoff
- Elektrolyse
- Bor
- Alkane
- Verbrennung Alkane
- Chlor
- Elektronegativität
- Tenside
- Toluol, Toluol Herstellung
- Wasserstoffbrückenbindung
- Fraktionierte Destillation Von Erdöl
- Carbonsäure
- Ester
- Harnstoff, Kohlensäure
- Reaktionsgleichung Aufstellen
- Redoxreaktion Übungen
- Stärke und Cellulose Chemie
- Süßwasser und Salzwasser
- Katalysator
- Ether
- Primärer Alkohol, Sekundärer Alkohol, Tertiärer Alkohol
- Van-der-Waals-Kräfte
- Oktettregel
- Kohlenstoffdioxid, Kohlenstoffmonoxid, Oxide
- Alfred Nobel
- Wassermolekül
- Ionenbindung
- Phosphor
- Saccharose Und Maltose
- Aldehyde
- Kohlenwasserstoff
- Kovalente Bindung
- Wasserhärte
- Peptidbindung
- Fermentation



























